Semaglutid
|
Produktname |
Semaglutid |
|
CAS Nr. |
910463 - 68 - 2 |
|
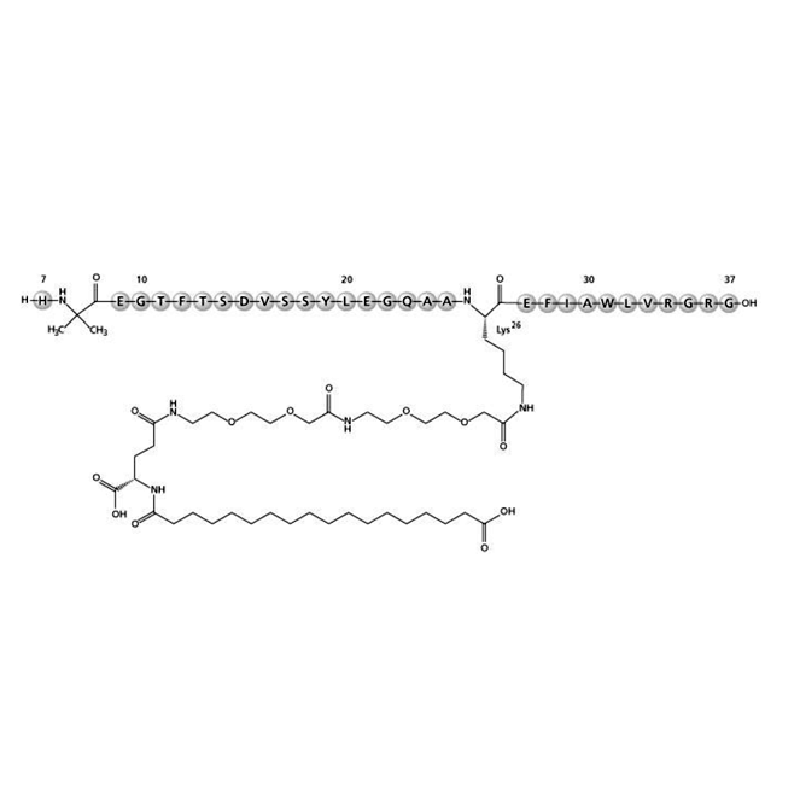
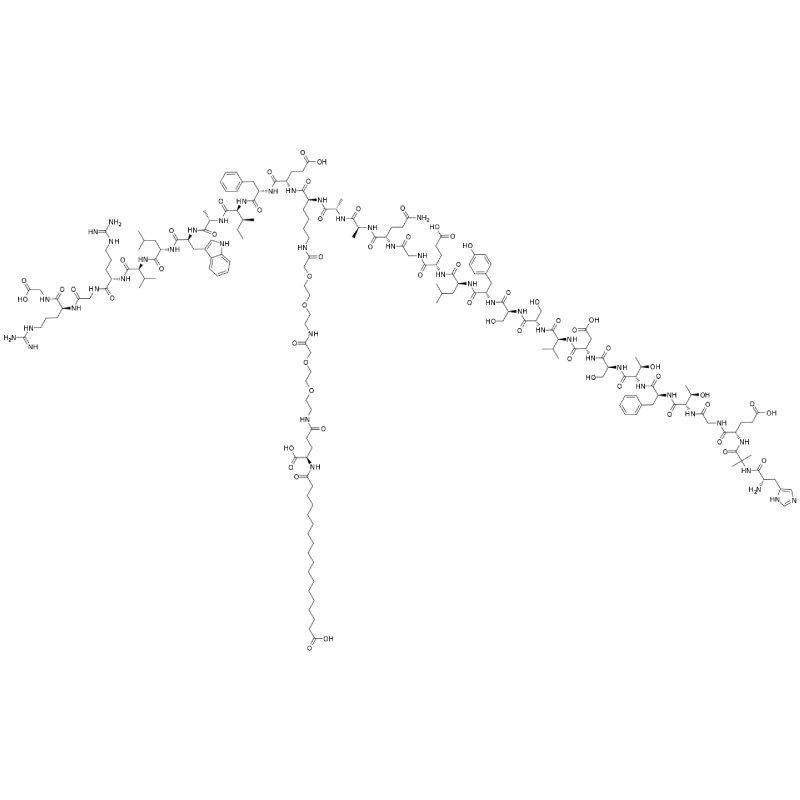
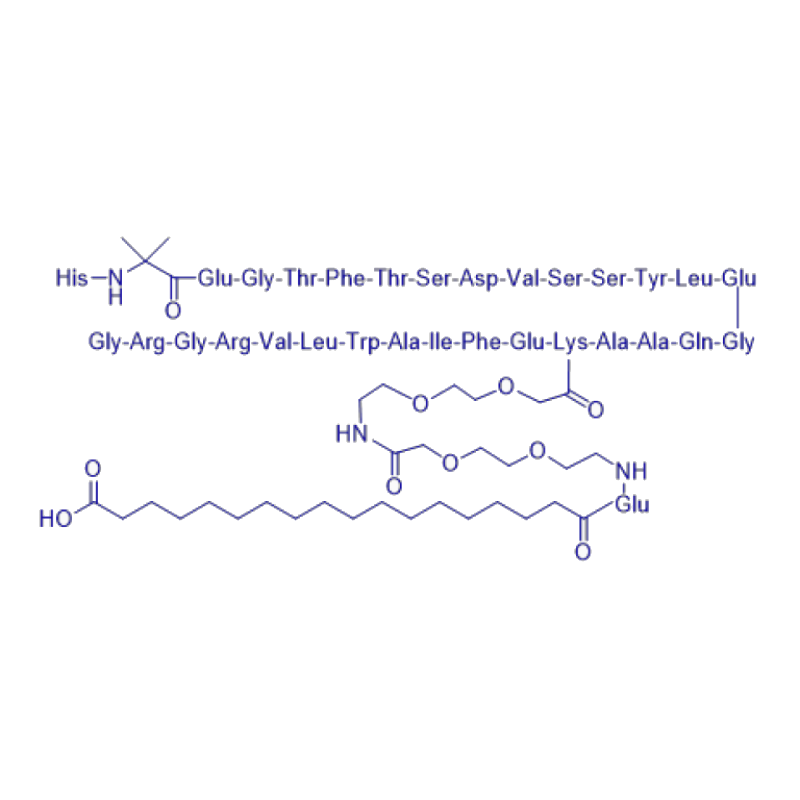
Sequenz |
Sein - aib - glu - gly - thr - phe - thr - ser - Asp - val - ser - ser - tyr - leu - glu - gly - gln - ala - ala - lys (peg2 - peg2 - γ γ - glu - |
|
Molekülformel |
C187H291N45O59 |
|
Molmasse |
4,113,58 da |
|
Reinheit |
/ |
|
Die maximal nicht spezifizierte Unreinheit |
≤ 0,1% |
|
Lagertemperatur |
2 - 8 ℃ |
|
Packgröße |
50g/Flasche oder bei Kundenanforderungen. |
Etikett:Semaglutidpeptid GLP - 1
Semaglutid ist ein langer - amtierender GLP - 1 Rezeptoragonist, der von Dänemarks Novo Nordisk nach Liraglutid auf den Markt gebracht wurde. Es ist der zweite GLP - 1 -Rezeptoragonist der Welt, um doppelte Indikationen für Fettleibigkeit und Typ -II -Diabetes zu erhalten. Im Vergleich zu Liraglutid hat Semaglutid eine längere Hälfte von 165 Stunden (fast 7 Tage) und kann einmal pro Woche injiziert werden. Semaglutid wurde erstmals am 5. Dezember 2017 in den USA eingeführt und im April 2021 in China ins Leben gerufen.
Semaglutid wird als Ergänzung zu Ernährung und Bewegung angezeigt, um die glykämische Kontrolle bei Patienten mit Typ -II -Diabetes zu verbessern. Es ist angezeigt, um wichtige nachteilige kardiovaskuläre Ereignisse (kardiovaskulärer Tod, nicht tödlicher Myokardinfarkt oder nicht tödlicher Schlaganfall) zu verringern. Darüber hinaus wurde am 4. Juni 2021 die Semaglutidinjektion (2,4 mg, einmal wöchentlich) von der US -FDA offiziell für das chronische Gewichtsmanagement bei fettleibigen oder übergewichtigen Erwachsenen zugelassen. Kürzlich hat die FDA den erweiterten Hinweis auf Semaglutid zur Behandlung von Fettleibigkeit bei Jugendlichen ab 12 Jahren zugelassen.
Am 10. Oktober 2023 kündigte Novo Nordisk die Ergebnisse der Semaglutid -Zwischenanalyse der Durchflussstudie zur Verhinderung der Nierenfunktionsstörung mit Diabetes -Patienten an. Die Ergebnisse zeigten, dass das Semaglutid bei der Verzögerung des Fortschreitens der chronischen Nierenerkrankung signifikant wirksam war und das unabhängige Datenüberwachungskomitee (DMC) anführte, um eine frühzeitige Beendigung der Studie auf der Grundlage spezifischer vorbestimmter Kriterien zu empfehlen.
Laut der von Novo Nordisk angekündigten Leistung verfügt Semaglutide über die herausragendsten Verkaufsdaten. Der Gesamtumsatz von 2022 betrug 10,9 Milliarden US -Dollar und einen Umsatz in China von 2,085 Mrd. RMB. Der Umsatz in den ersten drei Quartalen von 2023 hat 14,7 Milliarden US -Dollar überschritten, von denen das Gewichtsverlust -Medikament (Wegovy) ein Jahr lang eine Wachstumsrate von 481%hat, die Diabetes -Injektionsform (Ozempic) hat ein Jahr, das ein Jahr lang 53%und das Diabetes oral -dosage -Formen (RYBELS). Alle wachsen immer noch in einem schnellen Tempo, wobei der Umsatz mit vollem - Jahr voraussichtlich 20 Milliarden US -Dollar übersteigt.